2025е№ҙ6жңҲ2ж—ҘпјҢпјҢпјҢпјҢпјҢпјҢиҸ иҸңжӢ…дҝқзҪ‘пјҲ2696.HKпјүе®ЈеёғпјҢпјҢпјҢпјҢпјҢпјҢе…¬еҸёз«ӢејӮеһӢжҠ—HER2еҚ•жҠ—HLX22зҡ„жңҖж–°з ”з©¶ж•ҲжһңеңЁ2025е№ҙзҫҺеӣҪдёҙеәҠиӮҝзҳӨеӯҰдјҡпјҲASCOпјүе№ҙдјҡдёҠе®ЈеёғпјҢпјҢпјҢпјҢпјҢпјҢеҢ…жӢ¬HLX22иҒ”еҗҲжӣІеҰҘзҸ еҚ•жҠ—еҸҠеҢ–з–—дёҖзәҝжІ»з–—HER2йҳіжҖ§жҷҡжңҹиғғзҷҢзҡ„IIжңҹдёҙеәҠз ”з©¶пјҲHLX22-GC-201пјүзҡ„з–—ж•ҲдёҺжё…йқҷжҖ§и¶…дёӨе№ҙйҡҸи®ҝжӣҙж–°ж•°жҚ®пјҢпјҢпјҢпјҢпјҢпјҢд»ҘеҸҠеӨҙеҜ№еӨҙжҜ”з…§дёҖзәҝж ҮеҮҶз–—жі•пјҲжӣІеҰҘзҸ еҚ•жҠ—+еҢ–з–—Вұеё•еҚҡеҲ©зҸ еҚ•жҠ—пјүзҡ„еӣҪйҷ…еӨҡдёӯеҝғIIIжңҹдёҙеәҠз ”з©¶пјҲHLX22-GC-301пјүзҡ„з ”з©¶и®ҫи®ЎйҰ–ж¬Ўе®ЈеёғгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮHLX22-GC-201з ”з©¶жӣҙж–°ж•°жҚ®жҳҫзӨәпјҢпјҢпјҢпјҢпјҢпјҢз»Ҹз”ұжҒ’д№…йҡҸи®ҝпјҢпјҢпјҢпјҢпјҢпјҢHLX22еңЁHER2йҳіжҖ§иғғзҷҢжІ»з–—дёӯдҫқ然еұ•зҺ°еҮәзЁіеӣәзҡ„з–—ж•ҲиҺ·зӣҠпјҢпјҢпјҢпјҢпјҢпјҢиҝңи¶…еҺҶеҸІж•°жҚ®гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮHLX22-GC-301з ”з©¶жӯЈеңЁе…Ёзҗғ规模еҶ…й«ҳж•ҲжҺЁиҝӣ并已еңЁеӨҡең°е®ҢжҲҗйҰ–дҫӢжӮЈиҖ…з»ҷиҚҜгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮзҺ°еңЁпјҢпјҢпјҢпјҢпјҢпјҢе…Ёзҗғе°ҡж— еҗҢзұ»з”ЁдәҺжІ»з–—HER2йҳіжҖ§иғғзҷҢзҡ„HER2еҸҢйқ¶еҗ‘з–—жі•иҺ·жү№еҮҶдёҠеёӮгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮ

еҸҢйқ¶еҗ‘еҸҢиЎЁдҪҚиҝһзі»HER2пјҢпјҢпјҢпјҢпјҢпјҢзӘҒз ҙиғғзҷҢдёҖзәҝжІ»з–—жЎҺжўҸ
жҚ®GLOBOCANж•°жҚ®жҳҫзӨәпјҢпјҢпјҢпјҢпјҢпјҢ2022е№ҙе…ЁзҗғзәҰжңү100дёҮиғғзҷҢж–°еҸ‘з—…дҫӢпјҢпјҢпјҢпјҢпјҢпјҢйҖҫ66дёҮж®’е‘Ҫз—…дҫӢпјҢпјҢпјҢпјҢпјҢпјҢз–ҫз—…иӮ©иҙҹжіӣиө·жҳҫи‘—ең°еҢәдёҚе№іиЎЎ[1]пјҢпјҢпјҢпјҢпјҢпјҢз»„жҲҗдәҶдёҖеӨ§еә·еҒҘй—®йўҳгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮеӨ§йғҪиғғзҷҢжӮЈиҖ…ж—©жңҹз—ҮзҠ¶йҡҗеҢҝпјҢпјҢпјҢпјҢпјҢпјҢзЎ®иҜҠж—¶е·ІеӨ„дәҺз–ҫз—…жҷҡжңҹпјҢпјҢпјҢпјҢпјҢпјҢжҖ»дҪ“йў„еҗҺдёҚиүҜпјҢпјҢпјҢпјҢпјҢпјҢ5е№ҙз”ҹж¶ҜзҺҮд»…дёә6%[2,3]гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮеҸӘз®Ўиҝ‘е№ҙжқҘйқ¶еҗ‘жІ»з–—пјҲеҰӮжҠ—HER2иҚҜзү©пјүе’Ңе…Қз–«жЈҖжҹҘзӮ№жҠ‘еҲ¶еүӮпјҲеҰӮжҠ—PD-1/PD-L1еҚ•жҠ—пјүеңЁиғғзҷҢзҡ„жІ»з–—дёӯеҸ–еҫ—дәҶдёҖе®ҡеёҢжңӣ[4]пјҢпјҢпјҢпјҢпјҢпјҢдҪҶйүҙдәҺиҜҘз–ҫз—…е…·жңүй«ҳеәҰеҲҶеӯҗејӮиҙЁжҖ§пјҢпјҢпјҢпјҢпјҢпјҢе·®еҲ«дәҡеһӢжӮЈиҖ…еҜ№еҢ–з–—гҖҒйқ¶еҗ‘жІ»з–—е’Ңе…Қз–«жІ»з–—зҡ„еҸҚеә”е·®еҲ«жҳҫи‘—[5]гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮе…Қз–«жІ»з–—еұҖйҷҗдәҺPD-L1йҳіжҖ§дәәзҫӨпјҢпјҢпјҢпјҢпјҢпјҢдё”з–—ж•Ҳж”№е–„жңүйҷҗгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮиғғзҷҢе°Өе…¶жҳҜHER2йҳіжҖ§иғғзҷҢзҡ„ж•ҙдҪ“жІ»з–—д»ҚдҝқеӯҳйҮҚеӨ§зҡ„жңӘзҹҘи¶ізҡ„дёҙеәҠйңҖжұӮгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮ
HLX22жҳҜдёҖж¬ҫйқ¶еҗ‘HER2зҡ„з«ӢејӮеһӢеҚ•е…ӢйҡҶжҠ—дҪ“пјҢпјҢпјҢпјҢпјҢпјҢе·ІдәҺ2025е№ҙиҺ·еҫ—зҫҺеӣҪйЈҹзү©иҚҜе“Ғзӣ‘и§ҶжІ»зҗҶеұҖпјҲFDAпјүе’Ң欧зӣҹ委е‘ҳдјҡпјҲECпјүжҺҲдәҲзҡ„еӯӨе„ҝиҚҜиө„ж ји®Өе®ҡпјҲOrphan Drug Designation, ODDпјүпјҢпјҢпјҢпјҢпјҢпјҢз”ЁдәҺиғғзҷҢзҡ„жІ»з–—гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮHLX22еҸҜиҝһзі»еңЁHER2зҡ„иғһеӨ–дәҡз»“жһ„еҹҹIVпјҢпјҢпјҢпјҢпјҢпјҢдҪҶиҝһзі»иЎЁдҪҚдёҺжӣІеҰҘзҸ еҚ•жҠ—жңүжүҖе·®еҲ«пјҢпјҢпјҢпјҢпјҢпјҢдҪҝеҫ—иҜҘдә§е“ҒиғҪеӨҹдёҺжӣІеҰҘзҸ еҚ•жҠ—еҗҢж—¶иҝһзі»иҮіHER2пјҢпјҢпјҢпјҢпјҢпјҢжңүз”ЁеўһиҝӣHER2дәҢиҒҡдҪ“пјҲHER2еҗҢжәҗдәҢиҒҡдҪ“еҸҠHER2/EGFRејӮжәҗдәҢиҒҡдҪ“пјүзҡ„еҶ…еҗһе’ҢйҷҚи§ЈпјҢпјҢпјҢпјҢпјҢпјҢе°ҶHER2зҡ„еҶ…еҗһж•ҲзҺҮжҸҗй«ҳдәҶ40%-80%пјҢпјҢпјҢпјҢпјҢпјҢиҝӣиҖҢзҲҶеҸ‘жӣҙејәзҡ„HER2еҸ—дҪ“йҳ»ж–ӯж•ҲжһңгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮдёҙеәҠеүҚз ”з©¶жү№жіЁпјҢпјҢпјҢпјҢпјҢпјҢHLX22дёҺжӣІеҰҘзҸ еҚ•жҠ—иҒ”еҗҲжІ»з–—иғҪеӨҹеҚҸеҗҢжҠ‘еҲ¶иӮҝзҳӨз»Ҷиғһеўһж®–е’ҢиҜұеҜјз»ҶиғһеҮӢдәЎпјҢпјҢпјҢпјҢпјҢпјҢеңЁдҪ“еҶ…е’ҢдҪ“еӨ–еқҮдҪ“зҺ°еҮәеўһејәзҡ„жҠ—иӮҝзҳӨжҙ»жҖ§гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮ
IIжңҹз ”з©¶ж•°жҚ®дә®зӮ№пјҡи¶…2е№ҙйҡҸи®ҝпјҢпјҢпјҢпјҢпјҢпјҢжҳҫзқҖ延伸PFSе’ҢOS
HLX22иҒ”еҗҲжұүжӣІдјҳ®пјҲжӣІеҰҘзҸ еҚ•жҠ—пјҢпјҢпјҢпјҢпјҢпјҢзҫҺеӣҪе•Ҷе“ҒеҗҚпјҡHERCESSI??пјҢпјҢпјҢпјҢпјҢпјҢ欧жҙІе•Ҷе“ҒеҗҚпјҡZercepac®пјүжІ»з–—HER2йҳіжҖ§иғғзҷҢзҡ„IIжңҹдёҙеәҠз ”з©¶пјҲHLX22-GC-201пјүж•ҲжһңжҳҫзӨәпјҢпјҢпјҢпјҢпјҢпјҢеңЁжұүжӣІдјҳ®иҒ”з”ЁеҢ–з–—зҡ„еҹәзЎҖдёҠеҠ е…ҘHLX22еҸҜжҸҗй«ҳHER2йҳіжҖ§G/GEJзҷҢжӮЈиҖ…дёҖзәҝжІ»з–—зҡ„з”ҹж¶Ҝжңҹе’ҢжҠ—иӮҝзҳӨеҸҚеә”пјҢпјҢпјҢпјҢпјҢпјҢдё”жё…йқҷжҖ§еҸҜжҺ§пјҢпјҢпјҢпјҢпјҢпјҢжңүжңӣйҮҚеЎ‘жҷҡжңҹиғғзҷҢзҡ„дёҖзәҝж ҮеҮҶжІ»з–—гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮиҜҘз ”з©¶ж•Ҳжһңж•°жҚ®йҰ–ж¬Ўе®ЈеёғдәҺ2024е№ҙзҫҺеӣҪдёҙеәҠиӮҝзҳӨеӯҰдјҡиғғиӮ йҒ“иӮҝзҳӨй’»з ”дјҡпјҲASCO GIпјүпјҢпјҢпјҢпјҢпјҢпјҢеҺҘеҗҺиҜҘз ”з©¶ж•°жҚ®еҸҠж•°жҚ®жӣҙж–°дәҰеҲ’еҲҶиҺ·йҖүе®ЈеёғдәҺMedе’Ң2024е№ҙ欧жҙІиӮҝзҳӨеӯҰдјҡиғғиӮ йҒ“иӮҝзҳӨй’»з ”дјҡпјҲESMO GIпјүгҖҒ2025е№ҙзҫҺеӣҪдёҙеәҠиӮҝзҳӨеӯҰдјҡиғғиӮ йҒ“иӮҝзҳӨй’»з ”дјҡпјҲASCO GIпјү[6-9]пјҢпјҢпјҢпјҢпјҢпјҢеӨҡж¬ЎйӘҢиҜҒдәҶз ”з©¶ж•ҲжһңеҸҜйқ жҖ§зҡ„еҗҢж—¶пјҢпјҢпјҢпјҢпјҢпјҢжӣҙиҝӣдёҖжӯҘжҸҗеҚҮдәҶиҜҘз ”з©¶еңЁеӯҰжңҜз•Ңзҡ„еҪұе“ҚеҠӣгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮ
HLX22-GC-201з ”з©¶зәіе…ҘжңӘз»Ҹзі»з»ҹжІ»з–—зҡ„еұҖйғЁжҷҡжңҹжҲ–иҪ¬з§»жҖ§HER2йҳіжҖ§иғғ/иғғйЈҹз®Ўиҝһзі»йғЁзҷҢпјҲG/GEJCпјүжӮЈиҖ…пјҢпјҢпјҢпјҢпјҢпјҢжҢү1:1йҡҸжңәеҲҶжҙҫиҮіHLX22+жӣІеҰҘзҸ еҚ•жҠ—+XELOXз»„жҲ–ж…°и—үеүӮ+жӣІеҰҘзҸ еҚ•жҠ—+XELOXз»„пјҢпјҢпјҢпјҢпјҢпјҢжҜҸ3е‘ЁдёәдёҖдёӘжІ»з–—е‘ЁжңҹгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮдё»иҰҒз»ҲзӮ№дёәиҮӘеҠӣеҪұеғҸиҜ„估委е‘ҳдјҡпјҲIRRCпјүеҮӯиҜҒе®һдҪ“зҳӨиҜ„д»·ж ҮеҮҶпјҲRECIST v1.1пјүиҜ„дј°зҡ„ж— еёҢжңӣз”ҹж¶ҜжңҹпјҲPFSпјүе’Ңе®ўи§Ӯзј“и§ЈзҺҮпјҲORRпјүпјӣпјӣпјӣпјӣпјӣж¬ЎиҰҒз»ҲзӮ№еҢ…жӢ¬е…¶д»–з–—ж•ҲеҸҠжё…йқҷжҖ§жҢҮж ҮгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮ
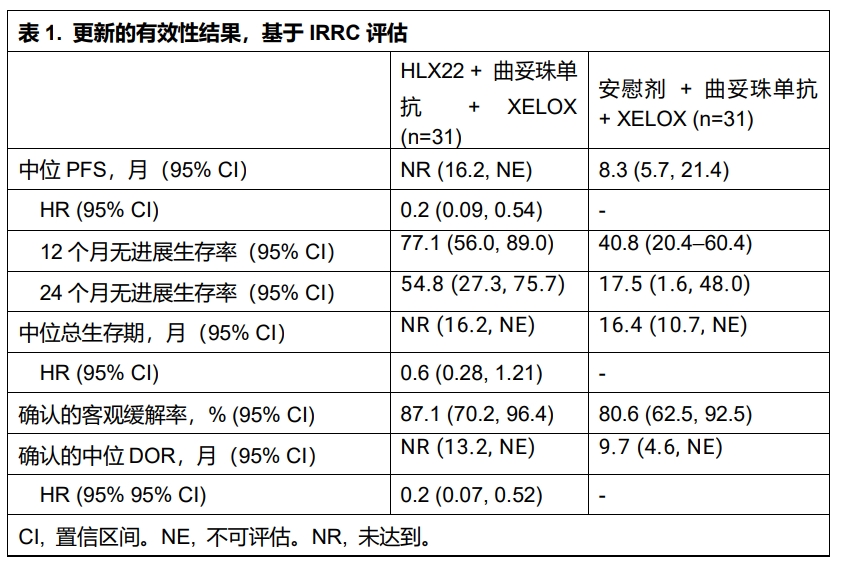
йҳ»жӯў2024е№ҙ12жңҲ6ж—ҘпјҢпјҢпјҢпјҢпјҢпјҢе…ұжңү62еҗҚжӮЈиҖ…иў«йҡҸжңәеҲҶз»„пјҲ31 vs 31пјүпјҢпјҢпјҢпјҢпјҢпјҢе…¶дёӯ51еҗҚпјҲ82.3%пјүдёәз”·жҖ§гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮдёӨз»„дёӯдҪҚйҡҸи®ҝе‘ЁжңҹеҲ’еҲҶдёә28.5дёӘжңҲе’Ң28.7дёӘжңҲгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮдё»иҰҒжңүз”ЁжҖ§ж•ҲжһңжӢңи§ҒиЎЁ1гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮдёӨз»„еҲ’еҲҶжңү30дҫӢпјҲ96.8%пјүе’Ң31дҫӢпјҲ100%пјүжӮЈиҖ…жҠҘе‘ҠдәҶжІ»з–—ж—¶д»ЈдёҚиүҜдәӢеҠЎпјҲTEAEsпјүгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮ17дҫӢпјҲ54.8%пјүе’Ң15дҫӢпјҲ48.4%пјүжӮЈиҖ…дёӯзҲҶеҸ‘дәҶ3зә§жҲ–д»ҘдёҠзҡ„TEAEsгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮж…°и—үеүӮ+жӣІеҰҘзҸ еҚ•жҠ—+XELOXз»„дёӯпјҢпјҢпјҢпјҢпјҢпјҢ1дҫӢпјҲ3.2%пјүжӮЈиҖ…зҲҶеҸ‘дәҶHLX22жҲ–ж…°и—үеүӮзӣёе…ізҡ„еҜјиҮҙж®’е‘Ҫзҡ„жІ»з–—жңҹдёҚиүҜдәӢеҠЎпјҲTEAEпјүгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮдёӨз»„еҗ„жңү1дҫӢжӮЈиҖ…пјҲ3.2%пјүжҠҘе‘ҠдёҺHLX22/ж…°и—үеүӮзӣёе…ізҡ„еҜјиҮҙжІ»з–—з»Ҳжӯўзҡ„TEAEгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮHLX22-GC-201з ”з©¶жӣҙж–°ж•ҲжһңеҶҚж¬Ўеә”иҜҒдәҶHLX22иҒ”еҗҲжӣІеҰҘзҸ еҚ•жҠ—еҸҠеҢ–з–—дёәHER2йҳіжҖ§G/GEJCжӮЈиҖ…еёҰжқҘжҳҫзқҖзҡ„дёҙеәҠиҺ·зӣҠпјҢпјҢпјҢпјҢпјҢпјҢдё”жё…йқҷжҖ§еҸҜжҺ§гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮ
IIIжңҹеӨҙеҜ№еӨҙз ”з©¶и®ҫи®ЎпјҡеӣҪйҷ…еӨҡдёӯеҝғиҜ•йӘҢе…ЁзҗғеҠ йҖҹжҺЁиҝӣ
еҹәдәҺеүҚзһ»жҖ§HLX22-GC-201з ”з©¶пјҢпјҢпјҢпјҢпјҢпјҢе…¬еҸёиҝӣдёҖжӯҘеңЁжӣҙеӨҡдәәзҫӨдёӯиҜ„д»·HLX22иҒ”еҗҲжӣІеҰҘзҸ еҚ•жҠ—еҸҠеҢ–з–—дёҖзәҝжІ»з–—HER2йҳіжҖ§жҷҡжңҹиғғзҷҢзҡ„з–—ж•ҲдёҺжё…йқҷжҖ§пјҢпјҢпјҢпјҢпјҢпјҢ并ејҖеұ•дёҖйЎ№еӨҙеҜ№еӨҙеӣҪйҷ…еӨҡдёӯеҝғIIIжңҹдёҙеәҠз ”з©¶пјҲHLX22-GC-301пјүгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮHLX22-GC-301з”ұеҢ—дә¬еӨ§еӯҰиӮҝзҳӨеҢ»йҷўжІҲзҗіе’ҢMDе®үеҫ·жЈ®зҷҢз—Үдёӯеҝғж•ҷжҺҲгҖҒNCCNиғғзҷҢдёҺйЈҹз®ЎзҷҢ专委дјҡдё»еёӯJaffer A. Ajaniж•ҷжҺҲй…ҚеҗҲжӢ…еҪ“зүөеӨҙдё»иҰҒз ”з©¶иҖ…гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮжӯӨж¬ЎASCOеӨ§дјҡйҰ–ж¬Ўе®ЈеёғHLX22-GC-301зҡ„иҜ•йӘҢи®ҫи®ЎпјҢпјҢпјҢпјҢпјҢпјҢиҜҘз ”з©¶жҳҜдёҖйЎ№йҡҸжңәгҖҒеҸҢзӣІгҖҒеҸҢиҮӮгҖҒеӣҪйҷ…еӨҡдёӯеҝғIIIжңҹдёҙеәҠиҜ•йӘҢпјҢпјҢпјҢпјҢпјҢпјҢж—ЁеңЁиҫғйҮҸHLX22иҒ”еҗҲжӣІеҰҘзҸ еҚ•жҠ—еҸҠXELOXи®ЎеҲ’дёҺжӣІеҰҘзҸ еҚ•жҠ—еҸҠXELOXиҒ”еҗҲжҲ–дёҚиҒ”еҗҲеё•еҚҡеҲ©зҸ еҚ•жҠ—дёҖзәҝжІ»з–—HER2йҳіжҖ§жҷҡжңҹиғғ/иғғйЈҹз®Ўиҝһзі»йғЁпјҲG/GEJпјүзҷҢзҡ„з–—ж•ҲдёҺжё…йқҷжҖ§гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮ
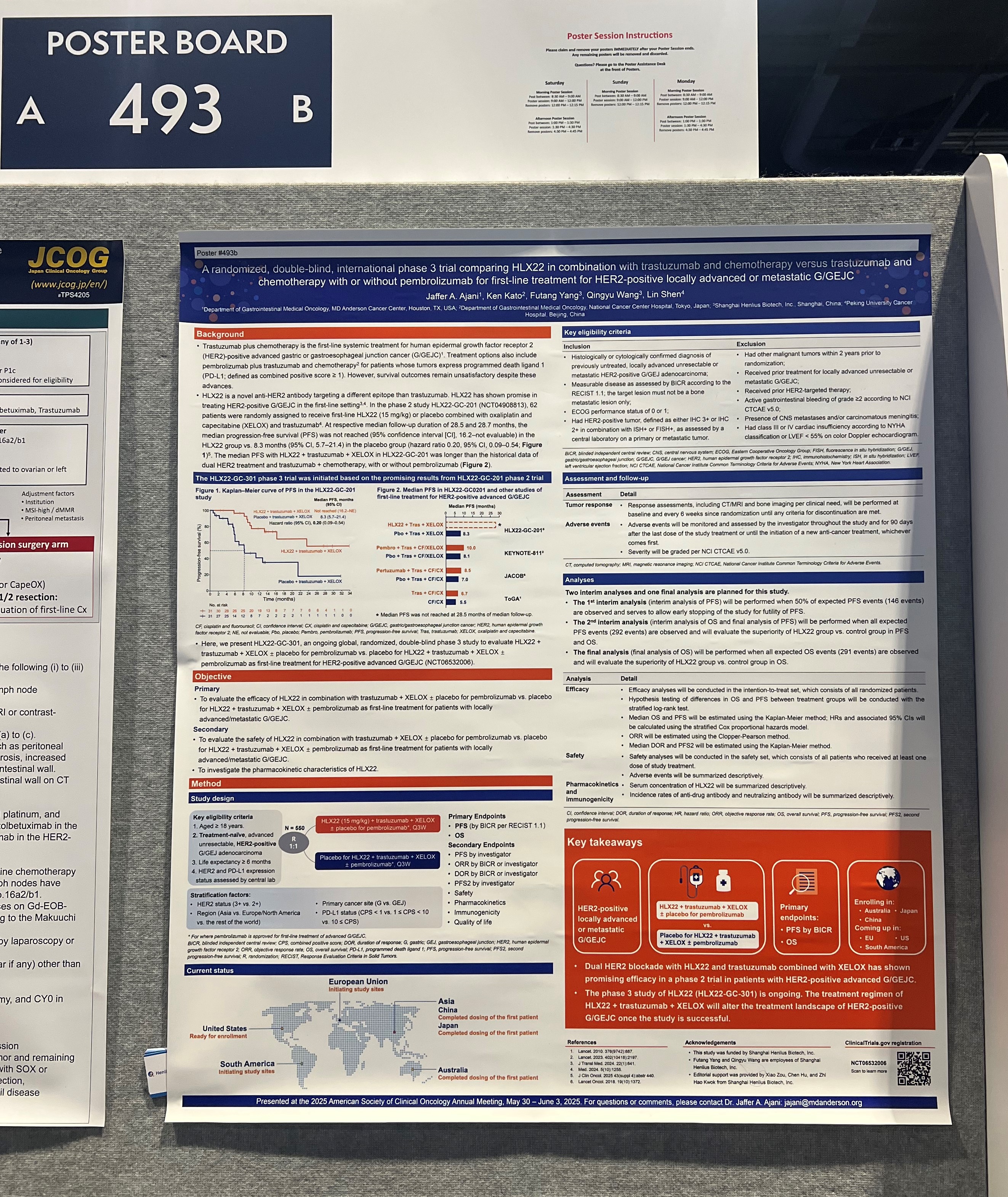
HLX22-GC-301иҰҒе®іе…ҘйҖүж ҮеҮҶеҢ…жӢ¬з»Ҹз»„з»ҮеӯҰжҲ–з»ҶиғһеӯҰзЎ®иҜҠгҖҒж—ўеҫҖжңӘжҺҘеҸ—жІ»з–—зҡ„еұҖйғЁжҷҡжңҹдёҚеҸҜеҲҮйҷӨжҲ–иҪ¬з§»жҖ§гҖҒHER2йҳіжҖ§G/GEJи…әзҷҢпјӣпјӣпјӣпјӣпјӣиҰҒе®іжү«йҷӨж ҮеҮҶеҢ…жӢ¬ж—ўеҫҖжҺҘеҸ—иҝҮд»»дҪ•HER2йқ¶еҗ‘жІ»з–—гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮз ”з©¶еҰ„жғід»Һе…ЁзҗғеӨҡдёӘең°еҢәе…Ҙз»„зәҰ550дҫӢжӮЈиҖ…пјҢпјҢпјҢпјҢпјҢпјҢжҢү1:1йҡҸжңәеҲҶжҙҫжҺҘеҸ—д»ҘдёӢжІ»з–—пјҡHLX22пјҲ15 mg/kgпјүиҒ”еҗҲжӣІеҰҘзҸ еҚ•жҠ—еҸҠXELOXВұеё•еҚҡеҲ©зҸ еҚ•жҠ—ж…°и—үеүӮпјҢпјҢпјҢпјҢпјҢпјҢжҲ–HLX22ж…°и—үеүӮиҒ”еҗҲжӣІеҰҘзҸ еҚ•жҠ—еҸҠXELOXВұеё•еҚҡеҲ©зҸ еҚ•жҠ—гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮHLX22зҡ„з»ҷиҚҜеңЁжҜҸдёӘ21еӨ©зҡ„жІ»з–—е‘Ёжңҹзҡ„第1еӨ©йҖҡиҝҮйқҷи„үиҫ“жіЁдёҫиЎҢпјҢпјҢпјҢпјҢпјҢпјҢдёҖиҝһз»ҷиҚҜиҮіжҚҹеӨұдёҙеәҠиҺ·зӣҠгҖҒж®’е‘ҪгҖҒжіӣиө·дёҚеҸҜиҖҗеҸ—жҜ’жҖ§гҖҒж’ӨеӣһзҹҘжғ…иөһжҲҗжҲ–е…¶д»–зјҳж•…еҺҹз”ұз»ҲжӯўгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮеҲҶеұӮеӣ зҙ еҢ…жӢ¬HER2е…Қз–«з»„еҢ–иҜ„еҲҶпјҲ3+зӣёжҜ”2+пјүгҖҒең°зҗҶеҢәеҹҹпјҲдәҡжҙІзӣёжҜ”欧жҙІ/еҢ—зҫҺзӣёжҜ”е…¶д»–ең°еҢәпјүгҖҒиӮҝзҳӨеҺҹеҸ‘йғЁдҪҚпјҲиғғзӣёжҜ”иғғйЈҹз®Ўиҝһзі»йғЁпјүеҸҠиӮҝзҳӨPD-L1иЎЁиҫҫпјҲCPS <1жҲ–дёҚеҸҜиҜ„дј°зӣёжҜ”1вүӨCPS<10зӣёжҜ”CPSвүҘ10пјүгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮй…ҚеҗҲдё»иҰҒз»ҲзӮ№дёәиҮӘеҠӣеҪұеғҸиҜ„估委е‘ҳдјҡеҹәдәҺе®һдҪ“зҳӨз–—ж•ҲиҜ„д»·ж ҮеҮҶпјҲRECIST v1.1пјүиҜ„дј°зҡ„ж— еёҢжңӣз”ҹж¶ҜжңҹпјҲPFSпјүпјҢпјҢпјҢпјҢпјҢпјҢд»ҘеҸҠжҖ»з”ҹж¶ҜжңҹпјҲOSпјүпјӣпјӣпјӣпјӣпјӣж¬ЎиҰҒз»ҲзӮ№еҢ…жӢ¬з ”究иҖ…иҜ„дј°зҡ„PFSгҖҒе®ўи§Ӯзј“и§ЈзҺҮгҖҒеҗҺз»ӯжІ»з–—зәҝзҡ„PFSгҖҒзј“и§ЈдёҖиҝһж—¶й—ҙгҖҒжё…йқҷжҖ§гҖҒиҚҜд»ЈеҠЁеҠӣеӯҰгҖҒе…Қз–«еҺҹжҖ§еҸҠз”ҹж¶ҜиҙЁйҮҸгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮ
еҖјеҫ—дёҖжҸҗзҡ„жҳҜпјҢпјҢпјҢпјҢпјҢпјҢHLX22-GC-301еҗҢжӯҘдәҺдёӯеӣҪгҖҒжҫіеӨ§еҲ©дәҡгҖҒ欧зӣҹгҖҒж—Ҙжң¬гҖҒзҫҺеӣҪгҖҒеҚ—зҫҺжҙІзӯүеӣҪ家е’Ңең°еҢәејҖи®ҫиҜ•йӘҢдёӯеҝғгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮйҳ»жӯўзҺ°еңЁпјҢпјҢпјҢпјҢпјҢпјҢиҜҘз ”з©¶е·ІдәҺдёӯеӣҪгҖҒж—Ҙжң¬гҖҒжҫіеӨ§еҲ©дәҡе®ҢжҲҗйҰ–дҫӢеҸ—иҜ•иҖ…з»ҷиҚҜпјҢпјҢпјҢпјҢпјҢпјҢ并已еңЁзҫҺеӣҪгҖҒжҷәеҲ©гҖҒйҹ©еӣҪзӯүеӣҪ家е’Ңең°еҢәиҺ·еҫ—дёҙеәҠиҜ•йӘҢејҖеұ•е…Ғи®ёгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮ
继HER2йҳіжҖ§иғғзҷҢд№ӢеҗҺпјҢпјҢпјҢпјҢпјҢпјҢHLX22зҡ„жІ»з–—йўҶеҹҹе·ІйҖҗжӯҘжӢ“е®ҪиҮід№іи…әзҷҢз–ҫз—…йўҶеҹҹгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮ2025е№ҙ4жңҲпјҢпјҢпјҢпјҢпјҢпјҢHLX22еҚ•жҠ—иҒ”еҗҲеҫ·жӣІеҰҘзҸ еҚ•жҠ—жІ»з–—HER2дҪҺиЎЁиҫҫHRйҳіжҖ§зҡ„еұҖйғЁжҷҡжңҹжҲ–иҪ¬з§»жҖ§д№іи…әзҷҢзҡ„IIжңҹдёҙеәҠз ”з©¶пјҲHLX22-BC201пјүдәҺдёӯеӣҪеўғеҶ…е®ҢжҲҗйҰ–дҫӢжӮЈиҖ…з»ҷиҚҜгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮHLX22иҒ”еҗҲеҫ·жӣІеҰҘзҸ еҚ•жҠ—зҡ„дёҙеәҠеүҚеҠЁзү©иҜ•йӘҢжҳҫзӨәпјҢпјҢпјҢпјҢпјҢпјҢиҜҘжҠ—HER2иҒ”еҗҲз–—жі•еұ•зҺ°еҮәеҚҸеҗҢжҠ—иӮҝзҳӨдҪңз”Ёе’ҢдјҳејӮзҡ„жё…йқҷжҖ§пјҢпјҢпјҢпјҢпјҢпјҢжңүжңӣдёәHER2иЎЁиҫҫиӮҝзҳӨжӮЈиҖ…еёҰжқҘжӣҙеӨҡиҺ·зӣҠгҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮжңӘжқҘпјҢпјҢпјҢпјҢпјҢпјҢиҸ иҸңжӢ…дҝқзҪ‘д№ҹе°ҶдёҖиҝһжҺўзҙўж–°еһӢжҠ—HER2йқ¶еҗ‘з–—жі•еңЁиӮҝзҳӨдёӯзҡ„жІ»з–—жҪңеҠӣпјҢпјҢпјҢпјҢпјҢпјҢй«ҳж•ҲжҺЁиҝӣHLX22зҡ„е…ЁзҗғдёҙеәҠејҖеҸ‘еёҢжңӣпјҢпјҢпјҢпјҢпјҢпјҢдёәе…ЁзҗғжӮЈиҖ…жҸҗдҫӣжӣҙеӨҡеҸҜиӮ©иҙҹгҖҒз–—ж•ҲжӣҙеҘҪзҡ„жІ»з–—и®ЎеҲ’гҖӮгҖӮгҖӮ
гҖӮгҖӮгҖӮгҖӮ
еҸӮиҖғж–ҮзҢ®
[1] Bray F, Laversanne M, Sung H, et al. CA Cancer J Clin. 2024: 1-35.
[2] Ajani JA. et al. J Natl Compr Canc Netw 2022;20(2):167-92.
[3] Alsina M. et al. Nat Rev Gastroenterol Hepatol 2023;20(3):155-70.
[4] Miao, ZF.,et al. Progress and remaining challenges in comprehensive gastric cancer treatment. Holist Integ Oncol 1, 4 (2022).
[5] Guan, WL.,et al. Gastric cancer treatment: recent progress and future perspectives. J Hematol Oncol 16, 57 (2023).
[6] Jin Li et al., HLX22 plus HLX02 and XELOX for first-line treatment of HER2-positive locally advanced or metastatic gastric/gastroesophageal junction cancer: A randomized, double-blind, multicenter phase 2 study.. JCO 42, 354-354(2024).DOI:10.1200/JCO.2024.42.3_suppl.354
[7] J. Li et al., 422P HLX22 plus HLX02 and XELOX as first-line therapy for HER2-positive advanced gastric/gastroesophageal junction cancer: Updated results from a randomized, double-blind phase II study, Annals of Oncology,Annals of Oncology (2024) 35 (suppl_1): S162-S204. 10.1016/annonc/annonc1482
[8] Li N, et al. A randomized phase 2 study of HLX22 plus trastuzumab biosimilar HLX02 and XELOX as first-line therapy for HER2-positive advanced gastric cancer. Med. 2024;5(10):1255-1265.e2.
[9] Jin Li et al. HLX22 plus trastuzumab and XELOX for first-line treatment of HER2-positive locally advanced or metastatic gastric/gastroesophageal junction cancer (G/GEJC): Updated results with additional patients.. JCO 43, 440-440(2025). DOI:10.1200/JCO.2025.43.4_suppl.440
